氨是一种重要的化工原料,广泛应用于农业、医药、化工等领域。氨的催化氧化是一种重要的氨化工反应,可以产生氮气和水,具有环保意义和经济效益。
1. 氨的氧化反应
氨的氧化反应是指氨在氧气存在下发生的化学反应,生成氮气和水。氨的催化氧化是一种重要的氨化工技术,在气体净化和氮气生产等领域有着重要的应用价值。催化氧化反应的方程式如下所示:
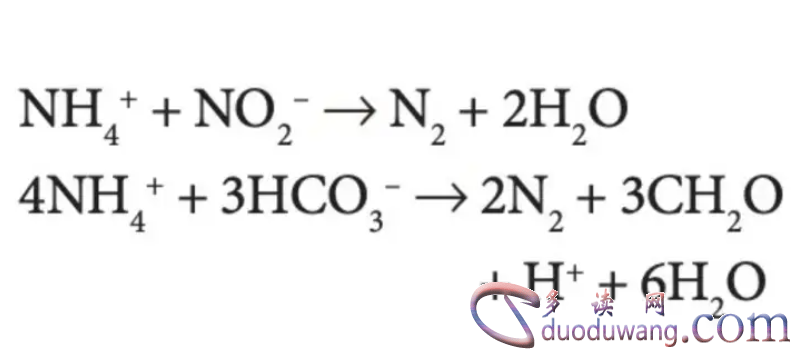
2NH3 + 3O2 → 2N2 + 3H2O
2. 催化剂的作用
在氨的催化氧化反应中,催化剂起着至关重要的作用。通常采用的催化剂包括铑、钌、铂等贵金属,它们能够促进氨与氧气的反应,提高反应速率和产率。催化剂在反应中不会被消耗,可以反复使用,具有较长的使用寿命。
3. 反应条件的影响
氨的催化氧化反应受到多种因素的影响,包括温度、压力、氨气和氧气浓度等。适当的反应条件可以提高反应效率和产品纯度。通常情况下,反应温度应控制在300-500摄氏度之间,反应压力在1-10大气压之间,气相中氨气和氧气的摩尔比也需要适当调节。
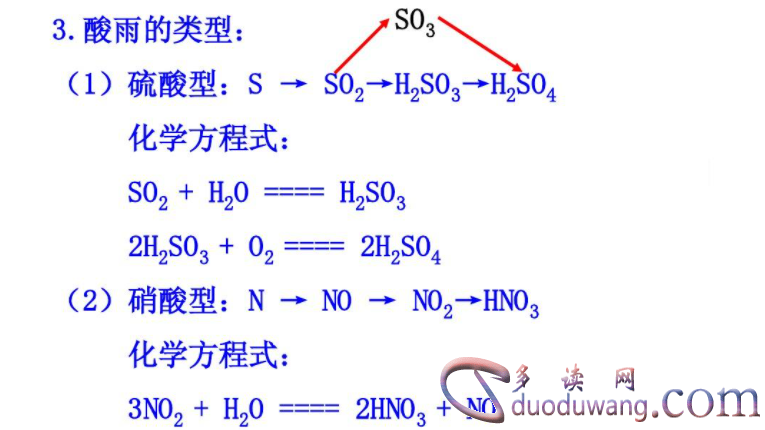
4. 工业应用
氨的氧化反应在工业生产中有着广泛的应用。例如,在氮气生产过程中,可以通过氨的催化氧化反应制备高纯度的氮气;在催化转化中,氨的氧化也是一种重要的反应过程。此外,氨的催化氧化还可以在废气净化等环境保护领域发挥重要作用。
5. 环保意义
氨的氧化反应能够产生无毒无害的氮气和水,不会产生有害气体和固体废物。因此,氨的催化氧化反应具有明显的环保意义,符合可持续发展的要求。在工业生产和废气处理领域广泛应用,有助于减少对环境的污染。
总结:氨的催化氧化是一种重要的氨化工技术,通过催化剂的作用促进氨与氧气的反应,产生氮气和水。在工业生产和环境保护领域有着重要的应用价值,具有明显的环保意义和经济效益。随着技术的不断进步和应用的拓展,氨的催化氧化将在未来发挥更为重要的作用,为促进绿色高效的工业发展做出贡献。